新聞中心Info
合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
-
> Delta-8使用新方法測試CMC,而不是表面張力測試法——方法
> 炔屬二醇表面活性劑對環(huán)氧灌漿材料漿液性能、灌體的滲透性影響(一)
> 微量天平和超微量天平定義、市場發(fā)展現狀及機遇
> 玻璃窗上水滴的運動控制影響因素及模型構建
> 3種不同變質煤樣經濕法超細粉碎后煤顆粒表面張力變化(二)
> ?界面流變儀可以測量液體表面張力嗎?界面流變儀與界面張力儀區(qū)別解析
> 超微量天平應用:錫灰中銀含量的分析檢測方法
> 陽-非離子復合表面活性劑體系表面張力測定及基礎性能評價(一)
> 磁化水表面張力是多少
> 定性分析聚合物界面張力與系統(tǒng)黏度比之間的關系——數值仿真結果、結論
推薦新聞Info
-
> 利用高通量表面張力儀探究三硅氧烷離子液體的吸附動力學
> 基于Delta-8表面張力儀的三硅氧烷離子液體動態(tài)吸附行為分析
> 偏硼酸鈉復配表面活性劑用于樁西高鈣鎂油藏超低界面張力驅油體系研究?
> 樁西原油與耐垢堿/表面活性劑復合體系的動態(tài)界面張力行為
> APTES在絹云母表面的周期性自組裝特性
> APTES/乙醇溶液處理與絹云母粉末表面張力測定
> 絹云母粉末表面APTES自組裝及其張力變化
> 堿是如何影響重烷基苯磺酸鹽體系的界面張力的?(二)
> 堿是如何影響重烷基苯磺酸鹽體系的界面張力的?(一)
> 羥基氨基改性硅油的合成、表面張力儀測試及其在炭纖維原絲油劑中的應用(三)
PH、結構、電荷與溫度對膠原生物表面活性劑溶液性質的影響機制(二)
來源: 《功能材料》 瀏覽 585 次 發(fā)布時間:2026-01-06
圖2為CBS溶液的表面張力-濃度對數(γ-lg C)曲線圖。從圖2可以看出,CBS溶液的表面張力在濃度對數為0.6時出現轉折點,<0.6時,其表面張力隨濃度對數的增加而急劇下降;>0.6時,CBS溶液的表面張力隨濃度對數的增加而出現平穩(wěn)狀態(tài)。因此,根據文獻描述的方法,判斷該轉折點為CBS溶液的臨界膠束濃度(CMC)的對數值。結合圖1可知,該轉折點對應的CBS溶液的濃度為4.0×10^-3 mg/mL,因此判斷CBS溶液的臨界膠束濃度為4.0×10^-3 mg/mL。在臨界膠束濃度以上,CBS分子已經形成有序組合體,溶液表面張力不再隨濃度的增大而增大。
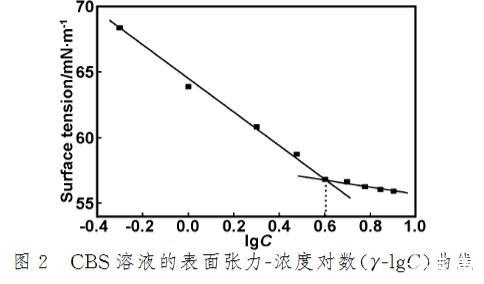
圖2 CBS溶液的表面張力-濃度對數(γ-lg C)曲線
3.1.2 pH值對CBS溶液表面張力的影響
Terashima等發(fā)現腐殖酸的平衡表面張力隨其溶液pH值的增大而向低濃度方向移動。Jeong等人考察含羞草種子蛋白提取液在不同pH值條件下的表面張力時,發(fā)現其表面張力分別在4.0、7.0和9.0時出現最低值。圖3即為CBS溶液在不同pH值條件下的表面張力曲線。從圖3可以看出濃度越大,表面張力值越低;隨著pH值的增大,CBS溶液的表面張力先降低而后增加;在pH值5.0時表面張力最小,分別為59.63(3.0×10^-3 mg/mL)、56.24(4.0×10^-3 mg/mL)和54.27 mN/m(5.0×10^-3 mg/mL)。Lin等認為明膠衍生物在酸性中的表面活性比堿性好的原因是疏水性增強以及凈負電荷降低造成的。此外,Lambert等在研究pH值對β-葡糖苷酶的表面張力的影響時,結果表明其表面張力值在pH值3.5時最小,與其等電點相近。CBS的等電點為4.93,因此,在pH值為5.0時,CBS分子聚集成有序的分子組合,且靜電荷最低,最終導致表面張力最低。
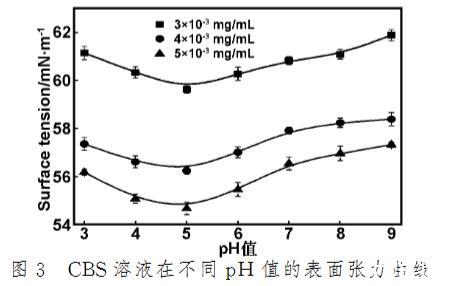
圖3 CBS溶液在不同pH值的表面張力曲線
3.1.3溫度對CBS溶液表面張力的影響
圖4所示為25~55℃下CBS溶液的表面張力曲線。由圖4可知,CBS濃度越大,表面張力值越低。在低溫下(≤35℃),表面張力相對較低,且保持平衡狀態(tài);在高溫下(>35℃),表面張力值較大,也保持平衡狀態(tài)。雖然在低溫下(≤35℃),溫度的升高能夠促進包埋在CBS分子中疏水殘基的暴露,但當溫度回復到20℃時其暴露的疏水殘基又被包埋進CBS分子內部,因此,低溫下并沒有出現表面張力的變化。然而,溫度繼續(xù)升高,使CBS分子變性,其三股螺旋結構受到破壞,大量親水基團裸露在外部且疏水作用減弱,這種變性具有不可逆性,因此在高溫下CBS溶液的表面張力急劇增大。由于CBS在高溫時已經變性,因此在高溫下其表面張力維持在較高值,且保持平緩狀態(tài)。
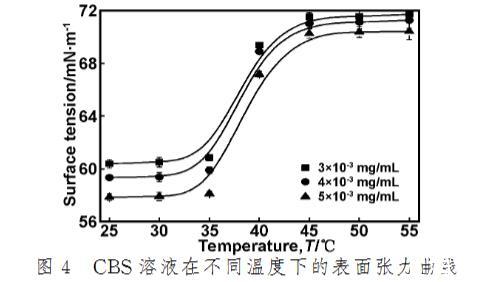
圖4 CBS溶液在不同溫度下的表面張力曲線
3.2 CBS溶液的表面吸附等溫線
通過γ-lg C曲線,應用Gibbs吸附(式(1))可求出不同濃度下CBS溶液的表面吸附量。當CBS的表面張力與其濃度對數呈線性關系時,由直線的斜率即可求出飽和吸附量(rm)。圖5即為CBS溶液在20℃時的γ-lg C線性擬合。
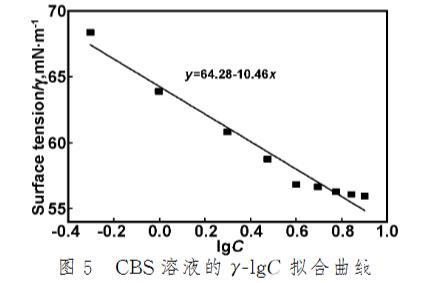
圖5 CBS溶液的γ-lg C擬合曲線
由圖5可知,CBS溶液的dγ/dlg C為負值,即表面張力隨濃度的增大而減小,CBS發(fā)生正吸附,也就是表面過剩為正值。這可能是因為隨著CBS濃度的增大,CBS分子向膠束內部轉移,使其微環(huán)境極性降低,從而導致發(fā)生正吸附。將擬合直線的斜率帶入式(1)計算出CBS溶液的飽和吸附量為1.86×10^-10 mol/cm^2。
對CBS溶液的表面張力-濃度(γ-C)進行對數擬合,可得到圖6所示的γ-C對數擬合曲線。根據γ-C擬合曲線以及Gibbs吸附公式可以作出不同溶液的吸附量對CBS溶液濃度的曲線,即吸附等溫線,如圖7所示。
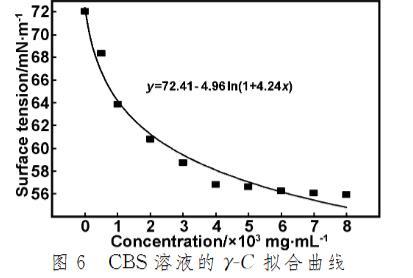
圖6 CBS溶液的γ-C擬合曲線
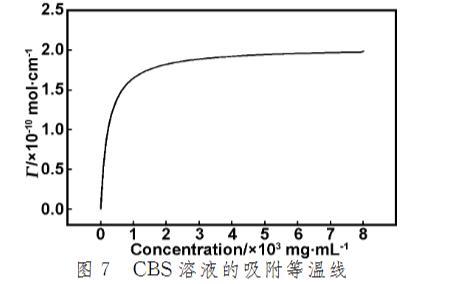
圖7 CBS溶液的吸附等溫線
從圖7可以看出,CBS溶液在低濃度時吸附量隨濃度的增加而呈線性增長,增長速率非常快。隨后增長速率降低并趨向穩(wěn)定,平穩(wěn)后的飽和吸附量為1.97×10^-10 mol/cm^2,與之前的計算結果(1.86×10^-10 mol/cm^2)相似,相應的表面張力也為最低值。
根據CBS溶液的吸附等溫線判定這類等溫線屬于Langmuir型等溫線,其數學表達式為
C/r=1/(rm k)+C/rm
式(2)中,r為Gibbs吸附量,rm為飽和吸附量,C為溶質濃度,k為吸附常數。以C/r對C作圖應得到一條直線,其斜率倒數即為飽和吸附量rm。圖8即為CBS溶液的C/r-C圖。從圖8可以計算出CBS溶液的飽和吸附量為2.03×10^-10 mol/cm^2,這與γ-lg C和r-C兩種曲線擬合的結果基本相等。
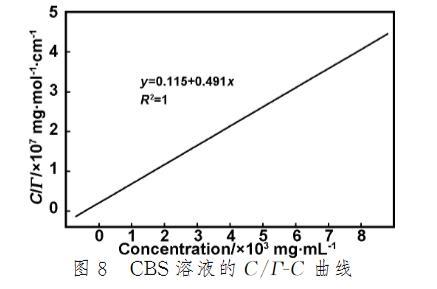
圖8 CBS溶液的C/r-C曲線
從圖8以及式(2)可以得到吸附常數k,也被稱為吸附平衡常數,與標準自由能ΔG^0有如下關系
k=exp(-ΔG^0/(RT))
由式(3)得到CBS溶液的標準吸附自由能為-3.53 kJ/mol,其標準自由能為負值,說明CBS溶液的表面吸附在標準狀態(tài)下能自發(fā)進行。
4結論
(1)CBS溶液的表面張力隨濃度的增大而降低,最后趨于平緩,此時表面張力為55.92 mN/m,并得出其臨界膠束濃度為4.0×10^-3 mg/mL。
(2)CBS溶液的表面張力隨pH的增大呈現先降低而后增加的趨勢,在等電點附近表面張力最小。
(3)CBS溶液的表面張力隨溫度的升高呈現兩種狀態(tài)。在低溫下,保持較好的表面活性,當溫度升高到一定程度(>35℃),由于變性作用,使得CBS的表面張力急劇增大。
(4)CBS溶液的吸附屬于Langmuir型吸附,根據γ-lg C擬合曲線、r-C擬合曲線以及C/r-C擬合曲線計算得到飽和吸附量相似,分別為1.86×10^-10、1.97×10^-10和2.03×10^-10 mol/cm^2。吸附自由能為-3.53 kJ/mol,為負值,在標準狀態(tài)下可以自由進行。










