合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
-
> 環保非水基鉆井液界面張力、基本性能和抗污染能力——前言、實驗部分
> 納米熔鹽形成機理、表面張力測定及影響因素研究(三)
> 過硫酸鉀、K2S2O8對壓裂液破膠性能與表面張力的影響——實驗部分
> 超微量天平應用實例:利用火試金法測定鉛精礦中銀含量
> 仲醇聚氧乙烯醚硫酸鹽平衡和動態表面張力及應用性能研究(二)
> 磺酸基團修飾水滑石LB復合薄膜自組裝機理及酸致變色特性(二)
> 溫度對水—十二烷基硫酸鈉體系與純水體系界面張力、厚度的影響——結果與討論、結論
> 純聚苯胺LB膜和聚苯胺與乙酸混合的LB膜制備、NO?氣體敏感特性研究(下)
> FYXF-3煤粉懸浮劑潤濕吸附性能、?傷害性能及在煤層氣壓裂改造現場的實施方案(一)
> 為什么鋼針會漂浮在水面上?
推薦新聞Info
利用高通量表面張力儀探究三硅氧烷離子液體的吸附動力學
來源:日用化學工業 瀏覽 23 次 發布時間:2026-04-13
2.2 短時吸附機理
當溶液濃度小于臨界膠束濃度時,溶液體相與次表面之間的傳質過程可以采用 Word-Tordai方程描述:
Γ(t) = 2c?√(Defft/π) - 2√(Deff/π) ∫?? cs d(√(t-τ))
式中 Γ(t) 為不同時刻表面過剩量,c? 為溶液的體相濃度,Deff 為表面活性劑的有效擴散系數,cs 為次表面濃度,t為時間,τ 為虛擬變量。式中前一項表示分子從體相向次表面的遷移,后一項表示隨著次表面濃度的增加,當次表面被分子全部占有時,分子將從次表面擴散回體相。然而式中后一項含有卷積積分,造成此方程不可解。
當溶液濃度很小時,γ(t) 接近于溶劑表面張力 γ?。在吸附的初始階段 t→0 時,次表面濃度 cs 很小,此時沒有分子從次表面返回體相,因此式(1)中第二項被省略,式(1)簡化為:
Γ(t) = 2c?√(Defft/π)
依據實驗結果,在吸附初始階段,γ(t)→γ?,有機硅離子液體水溶液可被看成稀溶液,因此,根據 Henry方程可得到 Γ 與 γ(t) 之間的關系:
γ(t) - γ? = -nRTΓ
式中,當表面活性劑為非離子型時,n=1;當為離子型時,n=2。將式(2)和式(3)結合可得:
γ(t)t→0 = γ? - 2nRTc?√(Deff/π) t1?2
因此,在短時間內,γ(t) 與 t1?2 呈線性關系,將γ(t) 與 t1?2 在短時內進行線性擬合,所得斜率即為-2nRTc?√(Deff/π),從而可計算出 Deff。
圖3是溫度為25℃時不同濃度[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液的γ(t)隨t1?2的變化和利用公式(4)線性擬合的結果。
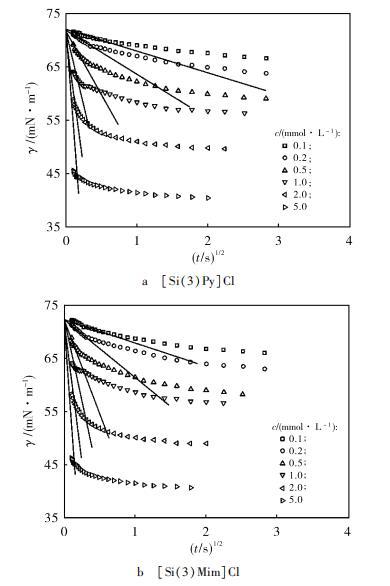
圖3 25℃時不同濃度有機硅離子液體水溶液的γ(t)與t1?2關系圖
從圖3可知,對于[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液,在濃度為0.1,0.2和0.5 mmol·L?1時,γ(t)與t1?2均在吸附初始階段呈線性關系。在濃度為1,2和5 mmol·L?1 2種溶液的γ(t)與t1?2在吸附初始階段內卻不能用式(4)進行擬合。測定值顯示,1,2和5 mmol·L?1 [Si(3)Py]Cl和[Si(3)Mim]Cl水溶液在儀器初始測量時表面張力已經小于65 mN·m?1,這表明此時吸附層中已經含有一定量有機硅離子液體分子。公式(3)是在假設吸附層作為稀溶液的情況下才成立的。此時高濃度情況下致使式(3)出現偏差,從而導致式(4)也不再適用。根據之前的研究,1,2和5 mmol·L?1 [Si(3)Py]Cl和[Si(3)Mim]Cl水溶液不能用式(4)擬合的主要原因可能是溶液表面中已經吸附的有機硅離子液體分子形成了雙電子層結構,該雙電子層結構產生的表面電荷成為吸附勢壘,從而影響了動態吸附過程。
圖4為0.5 mmol·L?1 [Si(3)Py]Cl和[Si(3)Mim]Cl水溶液在不同溫度下的γ(t)隨t1?2的變化曲線。在圖3和圖4線性擬合的基礎上,通過式(4)計算所得[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液不同濃度下或不同溫度下吸附初始階段的Deff列于表1中。從表1可知,對于稀溶液,在溫度一定時,隨著濃度的增加Deff變大,這是由于體相與次表面濃度差變大;在濃度一定時,隨著溫度的增加Deff變大,這是因為溫度的升高導致分子的熱運動加劇。
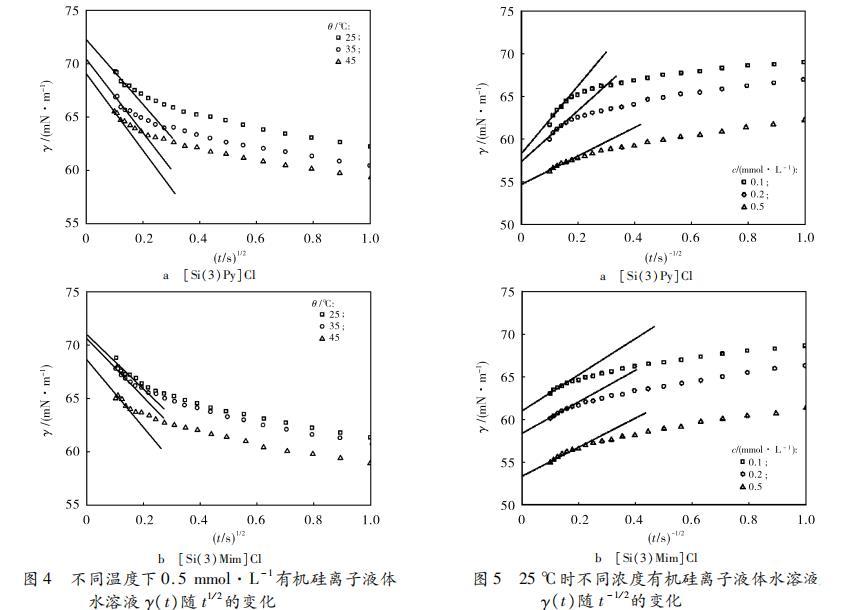
圖4 0.5 mmol·L?1有機硅離子液體水溶液在不同溫度下的γ(t)與t1?2關系圖
圖5 25℃時不同濃度有機硅離子液體水溶液的γ(t)與t?1?2關系圖
2.3 長時吸附機理
隨著吸附時間的增加,當 t→∞ 時,表面濃度逐漸趨近于體相濃度。假設此時擴散模型仍為擴散控制吸附機理,則:
Δct→∞ = c? - cs = Γ√(π/(4Dt))
式中 D為 t→∞ 時的擴散系數。
另外,Gibbs方程為:
dγ = -nRTΓ d ln c
將式(6)兩邊同時進行積分,并與式(5)結合可得:
γt→∞ = γeq + (nRTΓeq2 / c) √(π/(4Dt))
式中 Γeq 為平衡狀態下水溶液的表面過剩量。由式(7)可知,t→∞ 時,γ(t) 與 t?1?2 呈線性關系,將γ(t) 與 t?1?2 在 t?1?2→0 時內進行線性擬合,所得斜率即為 (nRTΓeq2 / c) √(π/(4D)),從而可計算出 D。圖5和圖6為不同測定條件下[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液的γ(t) 隨 t?1?2 的變化。
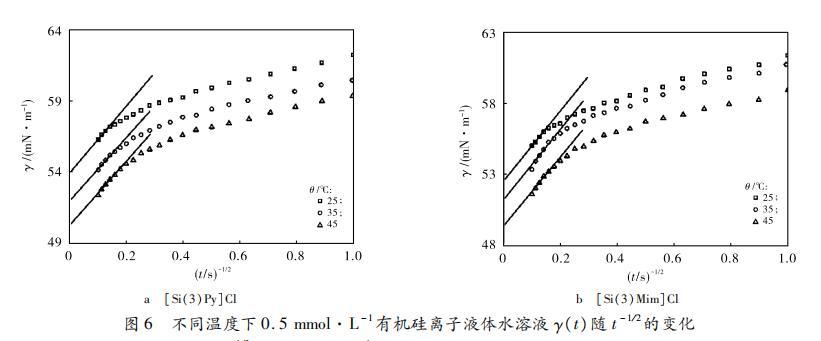
圖6 0.5 mmol·L?1有機硅離子液體水溶液在不同溫度下的γ(t)與t?1?2關系圖
根據式(7)對圖5和圖6進行線性擬合,計算所得不同測定條件下[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液長時吸附時的D列于表1中。由表1數據可知,在溫度一定時,隨著濃度的增加,D反而變小,這是因為此時次表面與體相的濃度差較小,濃度的增大導致分子間的靜電排斥作用變大,因此分子的自由運動受到一定的限制。然而,當濃度一定溫度變化時,隨著溫度升高,D逐漸變大,同樣也是由于溫度的增加致使分子熱運動加劇。表1中還列出各體系水溶液的 Deff/D,其范圍是8~255,說明兩階段的擴散系數相差較大,所有體系在整個吸附過程中都屬于混合動力控制吸附。
表1 不同測定條件下[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液的擴散系數
| 體系 | c?/(mmol·L?1) | θ/℃ | Deff/(m2·s?1) | D/(m2·s?1) | Deff/D |
|---|---|---|---|---|---|
| [Si(3)Py]Cl | 0.1 | 25 | 5.00×10?1? | 6.10×10?12 | 8.20 |
| 0.2 | 25 | 5.44×10?1? | 2.65×10?12 | 20.53 | |
| 0.5 | 25 | 6.90×10?11 | 2.98×10?13 | 231.54 | |
| 0.5 | 35 | 9.08×10?11 | 7.16×10?13 | 126.82 | |
| 0.5 | 45 | 1.16×10?1? | 7.28×10?13 | 159.34 | |
| [Si(3)Mim]Cl | 0.1 | 25 | 6.18×10?11 | 5.22×10?12 | 11.84 |
| 0.2 | 25 | 9.11×10?11 | 2.11×10?12 | 43.18 | |
| 0.5 | 25 | 9.58×10?11 | 3.89×10?13 | 246.27 | |
| 0.5 | 35 | 1.03×10?1? | 4.06×10?13 | 253.69 | |
| 0.5 | 45 | 1.08×10?1? | 4.25×10?13 | 254.12 |
3 結論
1)[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液動態表面張力均隨吸附時間的增加逐漸降低,直至恒定。在溫度一定的情況下,隨著濃度的增加,動態表面張力變小。
2)對于稀溶液,溫度一定時,在初始吸附階段Deff隨濃度增加而變大,而在長時吸附階段D隨濃度增加卻變小。然而濃度一定時,無論初始吸附階段還是長時吸附階段,二者均隨溫度增加而變大。
3)對于[Si(3)Py]Cl和[Si(3)Mim]Cl水溶液,在整個吸附過程中都屬于混合動力控制吸附。










